
Periode dan Golongan Unsur serta Sifatnya
Materi Kimia > Materi Kimia SMA > Sistem Periodik Unsur-Unsur.
Pertama kali kita akan mempelajari kimia, kita wajib tahu atom itu dan pengelompokkan unsurnya Sebab di artikel selanjutnya akan membahas yang berhubungan dengan Penggolongan unsur dan periodenya. Penggolongan unsur dan periode awalnya di ajukan oleh Dmitri Mandeleev yang membagikan gagasan di sistem periodik yang setelah itu dikembangkan lagi oleh Henry G. Moseley. Henry G. Moseley menyumbangkan nomer atom dan sempurnalah tabel periodik modern yang kita pake hingga sekarang ini.
Kali ini kita akan mempelajari mengenai Periode dan Golongan, Jadi persiapkan diri kalian.
Pertama kali kita akan mempelajari kimia, kita wajib tahu atom itu dan pengelompokkan unsurnya Sebab di artikel selanjutnya akan membahas yang berhubungan dengan Penggolongan unsur dan periodenya. Penggolongan unsur dan periode awalnya di ajukan oleh Dmitri Mandeleev yang membagikan gagasan di sistem periodik yang setelah itu dikembangkan lagi oleh Henry G. Moseley. Henry G. Moseley menyumbangkan nomer atom dan sempurnalah tabel periodik modern yang kita pake hingga sekarang ini.
Kali ini kita akan mempelajari mengenai Periode dan Golongan, Jadi persiapkan diri kalian.
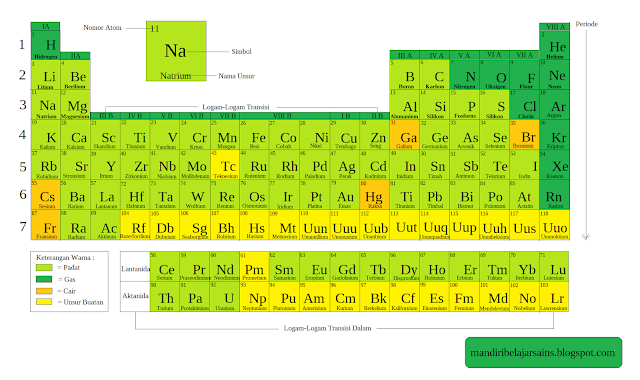 |
| Tabel Periodik |
1. Periode
Periode merupakan lajur-lajur horizontal dalam sistem periodik (pengulangan). Artinya periode akan ke bawah dalam pengurutannya, sesuai dengan jumlah periodiknya. Jumlah unsur di sistem periodik modern tidaklah sama setiap urutannya melainkan bertambah. Dalam sistem periodik modern kita mempunyai 7 periode. Bisa kita lihat tabel peride atau kita Bisa lihat di bawah ini untuk jumlah unsur setiap periode.
Periode 1 = 2 unsur
Periode 2 = 8 unsur
Periode 3 = 8 unsur
Periode 4 = 18 unsur
Periode 5 = 18 unsur
Periode 6 = 32 unsur
Periode 7 = 32 unsur
Periode merupakan lajur-lajur horizontal dalam sistem periodik (pengulangan). Artinya periode akan ke bawah dalam pengurutannya, sesuai dengan jumlah periodiknya. Jumlah unsur di sistem periodik modern tidaklah sama setiap urutannya melainkan bertambah. Dalam sistem periodik modern kita mempunyai 7 periode. Bisa kita lihat tabel peride atau kita Bisa lihat di bawah ini untuk jumlah unsur setiap periode.
Periode 1 = 2 unsur
Periode 2 = 8 unsur
Periode 3 = 8 unsur
Periode 4 = 18 unsur
Periode 5 = 18 unsur
Periode 6 = 32 unsur
Periode 7 = 32 unsur
Periode 1 hingga 3 disebut periode pendek, sedangkan periode 4 dan seterusnya disebut periode panjang. Itu pengenalan singkat mengenai periode.
2. Golongan
Golongan merupakan kolom-kolom vertikal dalam sistem periodik. Artinya, sistem periodik dibedakan dengan mendatar di tabel periodik. Coba lihat di tabel periodik.
Golongan yang berbeda mempunyai sifat yang berbeda, akan tetapi golongan yang sama mempunyai sifat yang sama. Jadi, dalam kimia penentuan sifat berdasarkan golongan.
di umumnya golongan mempunyai jumlah unsur yang sama Sebab dalam tabel periodik mempunyai jumlah 7 periode. akan tetapi untuk golongan unsur transisi dalam mempunyai jumlah unsur yang banyak seperti lantanida dan aktinida. Untuk lebih jelasnya kita pelajari yang mudah dulu.
Golongan merupakan kolom-kolom vertikal dalam sistem periodik. Artinya, sistem periodik dibedakan dengan mendatar di tabel periodik. Coba lihat di tabel periodik.
Golongan yang berbeda mempunyai sifat yang berbeda, akan tetapi golongan yang sama mempunyai sifat yang sama. Jadi, dalam kimia penentuan sifat berdasarkan golongan.
di umumnya golongan mempunyai jumlah unsur yang sama Sebab dalam tabel periodik mempunyai jumlah 7 periode. akan tetapi untuk golongan unsur transisi dalam mempunyai jumlah unsur yang banyak seperti lantanida dan aktinida. Untuk lebih jelasnya kita pelajari yang mudah dulu.
Ada dua bagian dari unsur yang termasuk sifat berbeda dalam bagian golongan, yaitu golongan A dan Golongan B. Coba kalian perhatikan bagus-bagus tabel periodik tersebut. Golongan B disebut juga unsur transisi. Dalam pembuatan tabel periodik, golongan IIIA wajib mencari sifat yang sama dengannya begitu pula untuk unsur golongan IIA Sebab golongan IIA dan IIIA memliki sifat yang sangat berbeda.
Sehingga unsur yang di dalam itu dimasukkan berdasarkan kemiripan IIIA. Jadi, unsur golongan B termasuk unsur peralihan Sebab mempunyai sifat yang sama dengan golongan IIIA walupun tak akan termasuk dalam golongan A.
Untuk Golongan A sebagian mempunyai nama, yaitu;
- Golongan IA : Logam Alkali (kecuali hidrogen)
- Golongan IIA ; Logam Alkali Tanah
- Golongan VIIA : Halogen
- Golongan VIIIA : Gas Mulia
Letak untuk golongan di sistem periodik ada di bawah ini
IA --- IIA --- IIIB --- IVB --- VB --- VIB --- VIIB --- IIXB --- IIXB --- IIXB --- IIB --- IIIB --- IIIA --- IVA --- VA --- VIA --- VIIA --- VIIIA
Golongan yang ditebali tersebut termasuk golongan Transisi. Urutan dari semuanya tak akan teratur bukan terutama untuk golongan transisi. Golongan IIXB mempunyai 3 golongan.
Golongan Transisi Dalam
Selain itu ada golongan dalam Golongan Transisi yaitu golongan transisi dalam.
Golongan transisi dalam ada dua antara lain, Lantanida dan Aktinida.
Lantanida merupakan unsur yang hampir mirip dengan Lantanum sehingga namanya disebut lantanida. Lantanida mempunyai nomor atom 57 - 70 yang terdiri atas 14 unsur. 14 unsur tersebut mempunyai sifat yang hampir sama dengan lantanum (Lihat Golongan IIB, periode 6).
Aktinida merupakan unsur yang hampir sama dengan Aktinium (lihat Golongan IIIB, Periode 7). Aktanida mempunyai nomor atom 89 - 102 yang terdiri atas 14 unsur. 14 unsur tersebut mempunyai sifat yang hampir sama dengan Aktinium.
Hubungan Konfigurasi Elektron dengan Sistem Periodik
Kita tahu bahwa sistem periodik modern yang dikembangkan oleh Henry G. Moseley telah membagikan sumbangan terhadap penentuan golongan berdasarkan nomor atom.
Moseley membuat itu berdasarkan sumbangan terdahulu oleh Mendeleev, yaitu berdasarkan massa atom relatf dan pembentukan golongan dan periode.
Semua itu untuk memudahkan dalam penentuan sifat-sifat unsur yang sama.
Dari table periodik kita dapatkan bahwa di nomor atom 1 mempunyai elektron valensi 1 dan golongannya 1, sedangkan di nomer atom 6 mempunyai elektron valensi 4 dan golongannya 4. Bisa kita simpulkan bahwa elektron velensi ditentukan berdasarkan golongannya. Sedangkan jumlah kulit ditentukan berdasarkan nomor periodenya. Nanti saya jelaskan lebih rinci di postingan selanjutnya.
Jadi kita Bisa ambil jawabanya seperti ini;
- Nomor Periode sama dengan jumlah kulit
- Nomor golongan sama dengan elektron valensi
Jadi, Jelas sekali ada hubungannya bukan.
Kita tahu bahwa sistem periodik modern yang dikembangkan oleh Henry G. Moseley telah membagikan sumbangan terhadap penentuan golongan berdasarkan nomor atom.
Moseley membuat itu berdasarkan sumbangan terdahulu oleh Mendeleev, yaitu berdasarkan massa atom relatf dan pembentukan golongan dan periode.
Semua itu untuk memudahkan dalam penentuan sifat-sifat unsur yang sama.
Dari table periodik kita dapatkan bahwa di nomor atom 1 mempunyai elektron valensi 1 dan golongannya 1, sedangkan di nomer atom 6 mempunyai elektron valensi 4 dan golongannya 4. Bisa kita simpulkan bahwa elektron velensi ditentukan berdasarkan golongannya. Sedangkan jumlah kulit ditentukan berdasarkan nomor periodenya. Nanti saya jelaskan lebih rinci di postingan selanjutnya.
Jadi kita Bisa ambil jawabanya seperti ini;
- Nomor Periode sama dengan jumlah kulit
- Nomor golongan sama dengan elektron valensi
Jadi, Jelas sekali ada hubungannya bukan.
Golongan unsur dan sifatnya;
Disini akan ditambahkan dengan masing-masing sifat dari unsur golongan A dan Golongan Transisi yang telah dinamai;
Unsur Golongan VIIIA (Gas Mulia)
Unsur-unsur golongan Gas mulia (Golongan VIIIA) terdiri dari Helium, Neon, Argon, Kripton, Ksenon, dan Radon. Unsur-unsur di golongan gas mulia sangatlah stabil dan Sebab stabil, jadi sangat sukar bereaktif dengan unsur lain. Itu semua Sebab konfigurasi elektronnya yang terisi penuh, Sifat lainnya merupakan energi ionisasinya yang sangat besar dan afinitas elektronnya yang sangat rendah, berupa gas. Selain itu gas mulia mempunyai titik cair dan titik didih yang sangat rendah.
Unsur Golongan VIIA (Halogen)
Halogen terdiri dari unsur-unsur Flour, Clorin, Bromium, Iodin, Astatin. Sifatnya bereaksi dengan logam membentuk garam. Keelektronegatifan tertinggi, jadi Halogen merupakan golongan paling non-logam. Unsur halogen umumnya berbentuk dwi-atom. Sifat lainnya merupakan berwarna dan bersifat racun. Contoh Senyawa yang terikat dengan Halogen NaBr, NaCl , dan NaI.
Unsur Golongan IA (Logam Alkali)
Golongan IA yang terdiri dari Litium, Natrium, Kalium, Rubidium, Sesium, dan Fransium (Kecuali Hidrogen). Sifat dari Logam Alkali merupakan sangat reaktif. Sebab sangat reaktif Alkali susah menemukan dalam bentuk tunggal (tak akan bergabung dengan unsur yang lain). Sifat alkali lainnya merupakan Bisa terbakar di udara, bereaksi hebat dengan air, dan termasuk logam yang ringan.
Unsur Golongan IIA (Logam Alkali Tanah)
Logam alkali tanah yang terdiri dari unsur Berilium, Magnesium, Kalsium, Stronsium, Barium, Radium. Sifat dari Logam Alkali Tanah merupakan Bisa membentuk basa dengan senyawa lain, akan tetapi kurang larut dengan air. Bisa ditemukan dalam tanah. Hampir sama sifatnya dengan Logam Alkali, yaitu mudah terbakar, logam aktif, akan tetapi dengan kereaktifannya kurang sehingga akan terbakar bila di udara bila dipanaskan.
Unsur Golongan Transisi
Logam transisi merupakan unsur yang terdiri dari golongan IIIB hingga IIB. Sifat dari logam transisi merupakan termasuk logam dan merupakan penghantar listrik yang bagus, massa jenis yang tinggi, dan titik didih dan titik leleh yang tinggi, banyak diantaranya membentuk senyawa yang berwarna.
0 Response to "Periode dan Golongan Unsur serta Sifatnya Yang wajib kita Ketahui"
Post a Comment